Mở đầu
Chào bạn! Có bao giờ bạn tự hỏi tại sao nghiên cứu về tế bào gốc trung mô (Mesenchymal stem cells – TBGTM) lại nhiều triển vọng đến thế? Bạn có biết rằng tế bào gốc từ dây rốn không chỉ giúp trẻ em khi mới sinh mà còn có thể mang lại những lợi ích không ngờ tới cho sức khỏe của người lớn? Hôm nay, chúng ta sẽ cùng tìm hiểu kỹ hơn về chủ đề này nhé!
Tham khảo chuyên môn
Bài viết này tham khảo thông tin từ Tiến sĩ Hoàng Minh Đức, Trưởng nhóm Dự án sản xuất thử nghiệm tại Viện Nghiên cứu Tế bào Gốc và Công nghệ gen Vinmec, cũng như các nghiên cứu khoa học từ các tạp chí uy tín như Exp Hematol, Biochem Soc Trans, và Cytotherapy.
Nội dung từ các bài viết trên VietMek.com chỉ mang tính chất tham khảo, không thay thế cho lời khuyên, chẩn đoán hoặc điều trị y tế chuyên nghiệp. Vui lòng tham khảo ý kiến bác sĩ hoặc chuyên gia y tế trước khi áp dụng bất kỳ thông tin nào từ bài viết này.
Tổng quan về Tế bào Gốc Trung Mô (TBGTM)
Khả năng tiềm năng của TBGTM
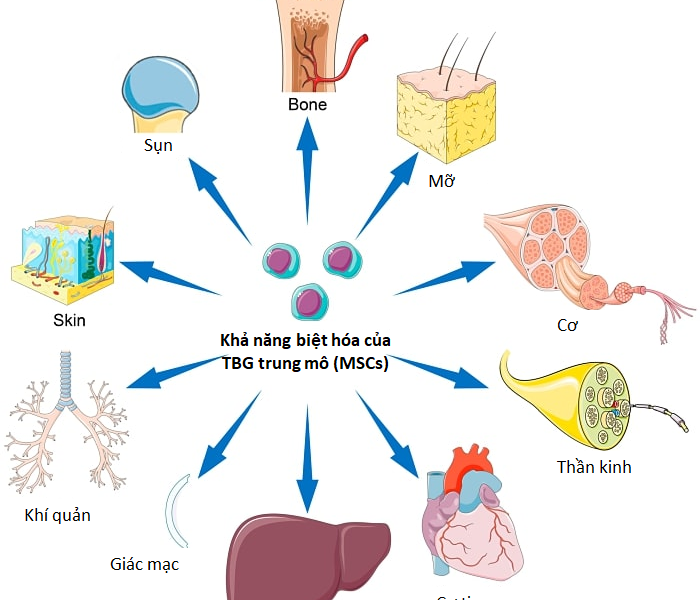
TBGTM là một loại tế bào có khả năng tái tạo, tự làm mới, điều hòa miễn dịch và có thể phát triển thành các loại tế bào khác như xương, sụn và mỡ. Được phát hiện đầu tiên bởi Friedenstein từ tủy xương vào năm 1976, TBGTM từ đó đã được tìm thấy ở nhiều nguồn khác nhau như mô mỡ, dây rốn và răng sữa [Friedenstein et al., 1976].
Ứng dụng và nghiên cứu về TBGTM
Nghiên cứu tiền lâm sàng trên mô hình động vật và trong phòng thí nghiệm đã chỉ ra các ứng dụng của TBGTM trong điều trị các bệnh qua khả năng điều hòa miễn dịch và tương tác cận tiết (paracrine) với các tế bào đích. Nhờ đó, TBGTM có thể tiếp cận các khu vực bị tổn thương qua cảm ứng từ cytokines viêm và tiết ra các chất tăng trưởng, giúp tái cấu trúc và phục hồi tại vị trí thương tổn.
Dây Rốn và TBGTM Từ Dây Rốn (TBGTMDR)
Sự hình thành và cấu tạo
Trong quá trình phát triển phôi thai, dây rốn được hình thành từ màng niệu nang sau thụ tinh và trở thành cấu nối giữa thai nhi và nhau thai. Dây rốn bao gồm ba phần chính: màng dây rốn, chất nhầy Wharton’s Jelly và các mạch máu (2 tĩnh mạch và 1 động mạch) [McElreavey et al., 1991]. Cụ thể hơn, Wharton’s Jelly có chức năng bảo vệ mạch máu, ngăn ngừa tắc nghẽn, xoắn vặn dây rốn.
Phát hiện về TBGTM từ dây rốn
Năm 1991, McElreavey và cộng sự đã phân lập thành công các tế bào dạng sợi từ Wharton’s Jelly, sau đó được xác định làTBGTM từ dây rốn (TBGTMDR). Các nghiên cứu mới đây cho thấy TBGTMDR có tốc độ tăng sinh và khả năng tự làm mới kéo dài hơn so với TBGTM từ tủy xương và mô mỡ. Điều này giúp TBGTMDR trở thành lựa chọn ưu tiên trong nhiều nghiên cứu và ứng dụng y tế [Hoang et al., 2021].
Các Đặc Điểm Sinh Học Của TBGTMDR
Khả năng tăng sinh và tự làm mới
TBGTMDR có khả năng tăng sinh và tự làm mới xuất sắc, được xử lý và nuôi cấy từ một lượng nhỏ dây rốn ban đầu. Với enzyme telomase hoạt động mạnh, các TBGTMDR có thể tăng sinh mà không làm thay đổi cấu trúc hệ gen, nhiễm sắc thể và kiểu hình của tế bào. Điều này mở ra cơ hội lớn cho việc thu thập và sử dụng TBGTMDR mà không gặp trở ngại về vấn đề đạo đức [Lu et al., 2006].
Đặc tính điều hòa miễn dịch
TBGTM và TBGTMDR có khả năng điều hòa miễn dịch xuất sắc, với khả năng kích ứng miễn dịch thấp do thiếu HLA-DR và biểu hiện thấp MHC nhóm I. Đặc biệt, TBGTMDR có khả năng ức chế miễn dịch mạnh hơn, không làm tăng sự thải ghép cấp tính và phù hợp cho phương pháp dị ghép đồng loài [Schnabel et al., 2014].
Ứng dụng thực tiễn và lợi ích của TBGTMDR
Điều trị các bệnh mãn tính và tự miễn
TBGTMDR đang được nghiên cứu để điều trị các bệnh mãn tính như xơ gan, tiểu đường và bệnh tim mạch. Cùng với khả năng điều hòa miễn dịch, các TBGTMDR có thể giúp giảm viêm, tái cấu trúc mô và khôi phục chức năng cho các cơ quan bị tổn thương [Yañez et al., 2006].
Điều trị các tổn thương và bệnh lý xương khớp
Nhờ khả năng biệt hóa và tái cấu trúc tế bào xương, sụn, TBGTMDR có tiềm năng lớn trong việc điều trị các tổn thương và bệnh lý liên quan đến xương khớp như thoái hóa khớp, chấn thương xương [Kita et al., 2010].
Các câu hỏi phổ biến liên quan đến tế bào gốc dây rốn
1. Tế bào gốc dây rốn khác gì so với tế bào gốc từ tủy xương?
Trả lời:
TBGTMDR có tốc độ tăng sinh và thời gian tự làm mới kéo dài hơn so với TBGTM lấy từ tủy xương.
Giải thích:
Điều này là do sự hoạt động mạnh của enzyme telomase trong tế bào TBGTMDR, giúp chúng tăng sinh mà không làm thay đổi gen hay nhiễm sắc thể, dẫn đến việc sử dụng được phổ biến hơn mà không gặp trở ngại về vấn đề đạo đức. Ngoài ra, việc thu thập TBGTMDR cũng dễ dàng hơn do không yêu cầu xâm lấn.
Hướng dẫn:
Nếu bạn cần tái tạo hoặc điều trị các bệnh mãn tính, việc lựa chọn TBGTMDR có thể là một sự lựa chọn tốt nhờ những ưu điểm của nó. Hãy thảo luận với bác sĩ chuyên khoa để có kế hoạch điều trị phù hợp.
2. Tế bào gốc từ dây rốn có thể điều trị bệnh gì?
Trả lời:
TBGTMDR có thể điều trị nhiều bệnh mãn tính và tự miễn như xơ gan, tiểu đường, và các bệnh lý về xương khớp.
Giải thích:
TBGTMDR có khả năng điều hòa miễn dịch, tái cấu trúc mô và khôi phục chức năng cho các cơ quan bị tổn thương. Khả năng này đã được chứng minh qua nhiều nghiên cứu khác nhau và đang dần được ứng dụng lâm sàng rộng rãi.
Hướng dẫn:
Để biết liệu bạn có thể sử dụng TBGTMDR cho bệnh lý của mình hay không, hãy thảo luận với bác sĩ hoặc các chuyên gia y tế. Đôi khi, sự tư vấn chuyên môn là cần thiết để đảm bảo hiệu quả và an toàn trong quá trình điều trị.
3. Có an toàn khi sử dụng tế bào gốc từ dây rốn?
Trả lời:
Có, việc sử dụng TBGTMDR là an toàn và đã được chứng minh qua nhiều nghiên cứu lâm sàng.
Giải thích:
Do thiếu HLA-DR và các marker kích hoạt miễn dịch CD80 và CD86, TBGTMDR không làm tăng nguy cơ thải ghép và phù hợp cho phương pháp dị ghép đồng loài. Các tế bào này cũng không làm thay đổi cấu trúc hệ gen qua các lần cấy chuyển, đảm bảo tính an toàn.
Hướng dẫn:
Nếu bạn cân nhắc sử dụng TBGTMDR cho mục đích điều trị, hãy tham khảo ý kiến bác sĩ. Điểm mạnh của loại tế bào này là an toàn và có thể giảm nguy cơ thải ghép, nhưng luôn cần sự tư vấn y tế trước khi sử dụng.
4. Tế bào gốc từ dây rốn có thể biệt hóa thành loại tế bào nào?
Trả lời:
TBGTMDR có thể biệt hóa thành nhiều loại tế bào khác nhau như tế bào xương, sụn, và tế bào mỡ.
Giải thích:
Nhờ khả năng tự làm mới và tái tạo, TBGTMDR có thể biệt hóa thành các loại tế bào khác nhau thuộc lớp trung mô. Điều này mở ra các ứng dụng tiềm năng trong việc tái tạo các mô và cơ quan bị tổn thương.
Hướng dẫn:
Nếu bạn muốn biết thêm về khả năng biệt hóa và ứng dụng của TBGTMDR trong điều trị, bạn nên đọc thêm các nghiên cứu và tham khảo ý kiến của bác sĩ chuyên khoa. Các thông tin này sẽ giúp bạn hiểu rõ hơn về lợi ích và khả năng của loại tế bào gốc này.
5. Việc lưu trữ tế bào gốc từ dây rốn có lợi ích gì?
Trả lời:
Việc lưu trữ tế bào gốc từ dây rốn có lợi ích lớn trong việc sẵn sàng tế bào gốc cho các phương pháp điều trị trong tương lai.
Giải thích:
Việc lưu trữ tế bào gốc từ dây rốn giúp có sẵn các tế bào gốc chất lượng cao khi cần thiết, cho phép các phương pháp điều trị nhanh chóng và hiệu quả hơn. Điều này đặc biệt hữu ích trong các tình huống cần can thiệp y tế nhanh chóng.
Hướng dẫn:
Nếu bạn đang cân nhắc việc lưu trữ tế bào gốc từ dây rốn, hãy liên hệ với các trung tâm y tế uy tín để được tư vấn. Điều này sẽ giúp bạn nắm bắt cơ hội sử dụng các công nghệ tế bào gốc tiên tiến nhất khi cần thiết.
Kết luận và khuyến nghị
Kết luận
Tế bào gốc từ dây rốn, đặc biệt là TBGTMDR, mang lại nhiều tiềm năng trong y học hiện đại. Từ khả năng tự làm mới, tăng sinh mạnh mẽ đến khả năng biệt hóa thành nhiều loại tế bào khác nhau, TBGTMDR mở ra nhiều triển vọng trong việc điều trị các bệnh mãn tính, bệnh tự miễn và tổn thương mô.
Khuyến nghị
Chúng tôi khuyên bạn nên tìm hiểu thêm về tế bào gốc từ dây rốn và thảo luận với các chuyên gia y tế để có cái nhìn toàn diện và đúng đắn nhất. Việc lưu trữ tế bào gốc từ dây rốn có thể là một quyết định sáng suốt, mang lại lợi ích lớn cho sức khỏe hiện tại và tương lai của bạn và người thân.
Tài liệu tham khảo
- Friedenstein AJ, Gorskaja JF, Kulagina NN. (1976). Fibroblast precursors in normal and irradiated mouse hematopoietic organs. Exp Hematol; 4(5):267-274.
- McElreavey KD, Irvine AI, Ennis KT, et al. (1991). Isolation, culture and characterisation of fibroblast-like cells derived from the Wharton’s jelly portion of human umbilical cord. Biochem Soc Trans; 19(1):29S.
- Hoang VT, Trinh QM, Phuong DTM, et al. (2021). Standardized xeno- and serum-free culture platform enables large-scale expansion of high-quality mesenchymal stem/stromal cells from perinatal and adult tissue sources. Cytotherapy; 23(1):88-99.
- Lu LL, Liu YJ, Yang SG, et al. (2006). Isolation and characterization of human umbilical cord mesenchymal stem cells with hematopoiesis-supportive function and other potentials. Haematologica; 91(8):1017-1026.
- Fong CY, Chak LL, Biswas A, et al. (2011). Human Wharton’s jelly stem cells have unique transcriptome profiles compared to human embryonic stem cells and other mesenchymal stem cells. Stem Cell Rev; 7(1):1-16.
- Bieback K, Brinkmann I. (2010). Mesenchymal stromal cells from human perinatal tissues: From biology to cell therapy. World J Stem Cells; 2(4):81-92.
- Schnabel LV, Pezzanite LM, Antczak DF, et al. (2014). Equine bone marrow-derived mesenchymal stromal cells are heterogeneous in MHC class II expression and capable of inciting an immune response in vitro. Stem Cell Res Ther; 5(1):13.
- Yañez R, Lamana ML, García-Castro J, et al. (2006). Adipose tissue-derived mesenchymal stem cells have in vivo immunosuppressive properties applicable for the control of the graft-versus-host disease. Stem Cells; 24(11):2582-2591.
- Kita K, Gauglitz GG, Phan TT, et al. (2010). Isolation and characterization of mesenchymal stem cells from the sub-amniotic human umbilical cord lining membrane. Stem Cells Dev; 19(4):491-502.
- Cagliani J, Grande D, Molmenti EP, et al. (2017). Immunomodulation by Mesenchymal Stromal Cells and Their Clinical Applications. J Stem Cell Regen Biol; 3(2).